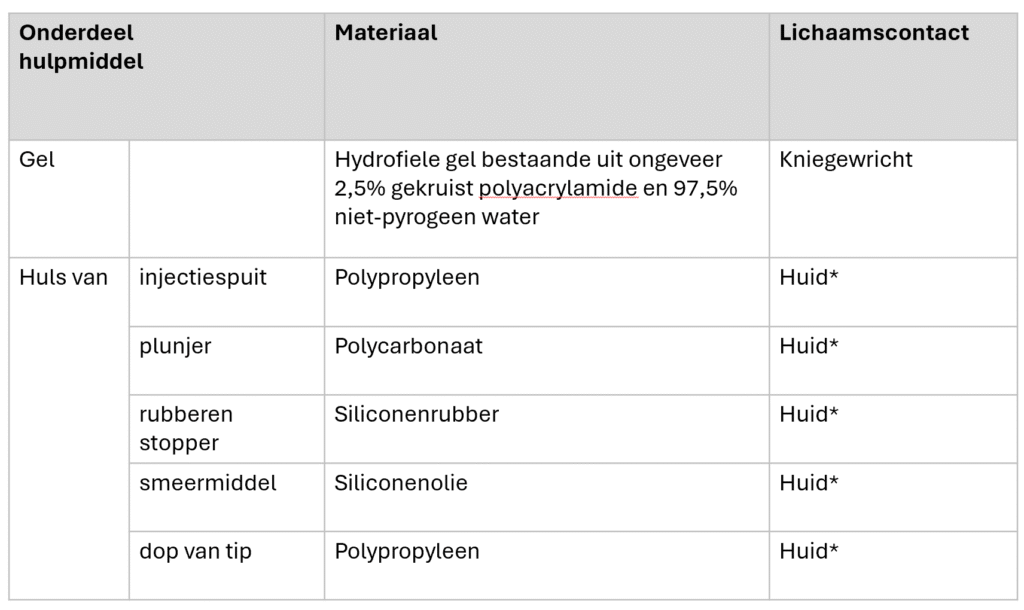
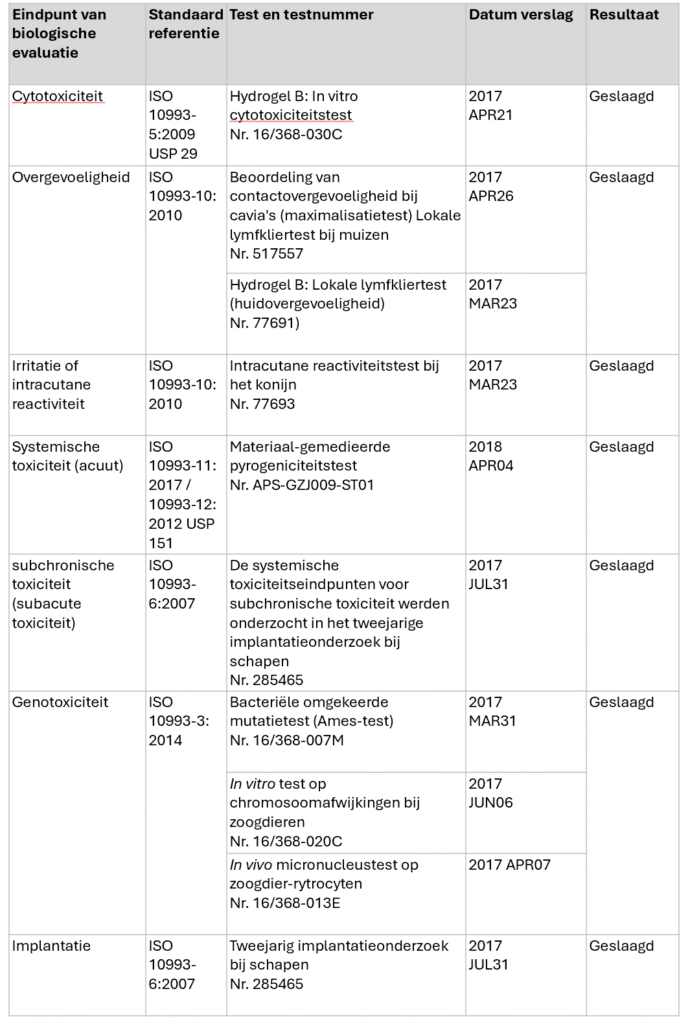
Comme décrit ci-dessus, l’hydrogel Arthrosamid®est composé de 2,5 % de matière sèche de polyacrylamide réticulé et de 97,5 % d’eau apyrogène. Lors de la synthèse, le N,N, méthylène-bis-acrylamide polymérise avec l’acrylamide, formant des liaisons transversales entre les chaînes de polyacrylamide.
L’hydrogel de polyacrylamide réticulé est synthétisé par un processus de polymérisation dans lequel des unités répétitives d’acrylamide sont liées entre elles par une réaction en chaîne.
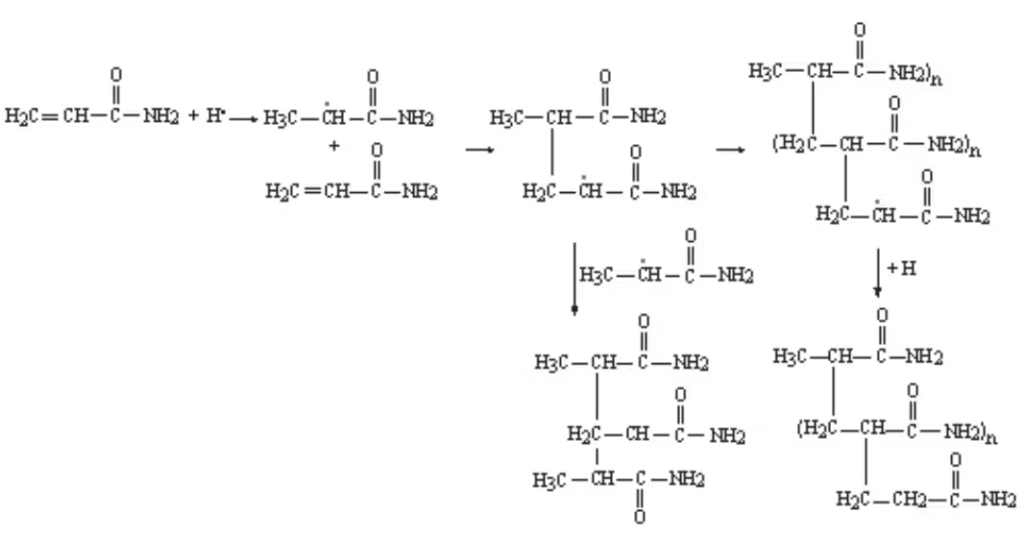
La réaction en chaîne utilise un principe d’initiateur redox, dans lequel un initiateur de persulfate d’ammonium (AMPS) génère un radical libre qui ajoute un monomère d’acrylamide en obtenant un électron de la double liaison dans l’acrylamide, formant une seule liaison carbone-carbone avec l’acrylamide. Cela laisse un électron non divisé pour l’ajout ultérieur de monomères d’acrylamide, comme le montre la figure 2 à droite.
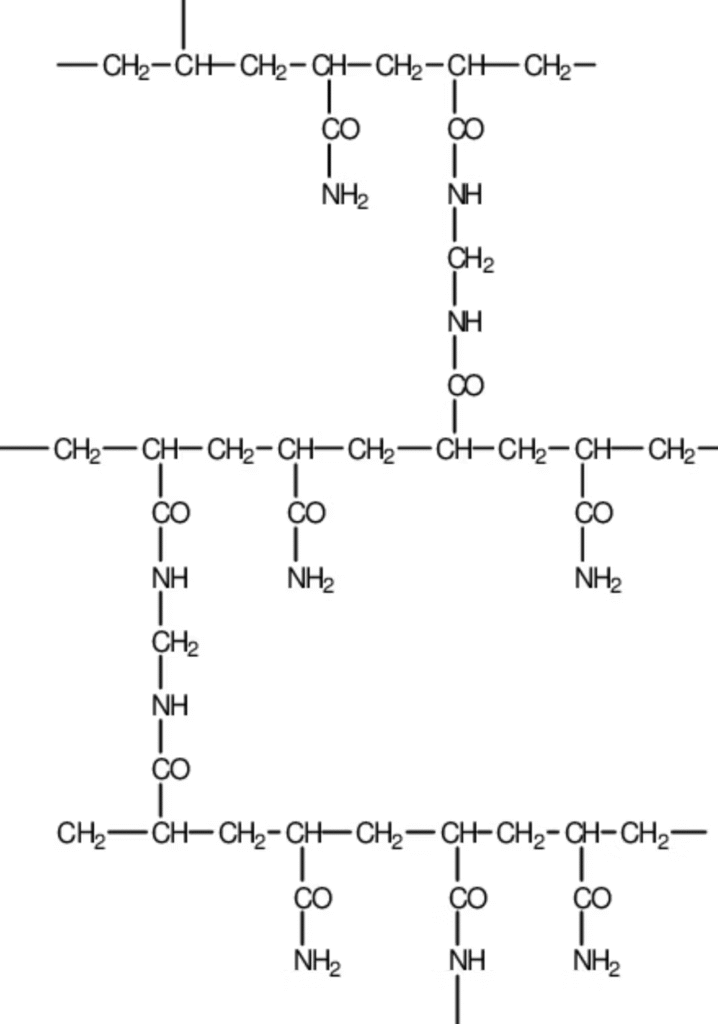
La ramification de la structure carbone-carbone linéaire du polyacrylamide se produit en raison de la présence d’un agent réticulé, le monomère N,N-méthylène-bis-acrylamide (MBAM), comme le montre la figure 3.
Après ramification des chaînes de polyacrylamide de la structure, un réseau tridimensionnel de polyacrylamide croisé est formé, au lieu de chaînes linéaires de polyacrylamide non couplées.
Arthrosamid® se présente sous la forme d’une seringue stérile préremplie de 1 ml à usage unique, munie d’un raccord luer lock et d’un capuchon d’étanchéité. Le médicament est destiné à être injecté par voie intra-articulaire dans l’articulation du genou à l’aide d’une aiguille stérile de 21G x 2 pouces (0,8 x 50 mm).
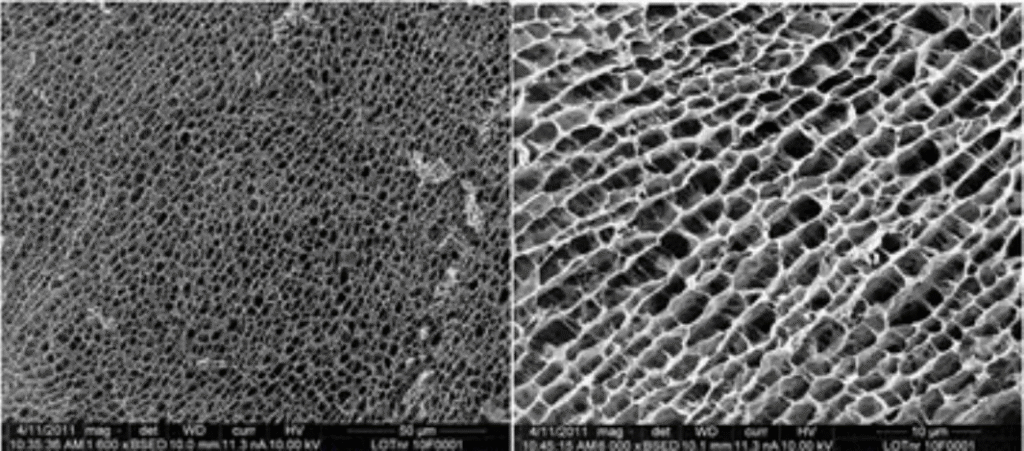
La figure 1 montre la structure tridimensionnelle de l’hydrogel de polyacrylamide. La structure en nid d’abeille uniforme et serrée fournit une grille pour la croissance des cellules.